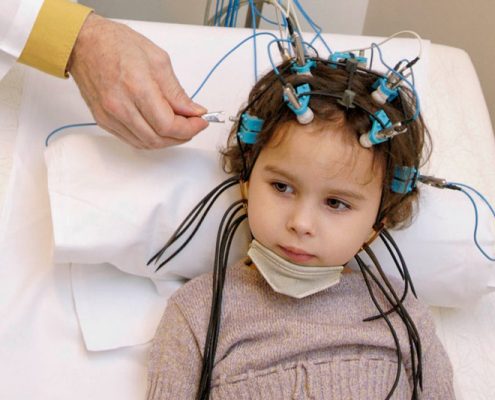
بیماری شارکو-ماری-توث
نوروپاتی چه تعریفی دارد؟
سیستم اعصاب محیطی شامل رشته های عصبی حسی و حرکتی هستند که حس اندام ها را به سیستم اعصاب مرکزی شامل مغز و نخاع می رسانند و دستورات حرکتی مغز و نخاع را به کل بدن می رسانند. نوروپاتی یعنی آسیب و ضایعه در سیستم اعصاب محیطی بدن که با علایم ضعف اندام، بی حسی یا درد در دست یا پا ظاهر می شود. نوروپاتی علل مختلفی مانند آسیب ضربه ای یا تروما، عفونت ها، بیماری های متابولیک و بیماری های ژنتیک دارد. دو نوع شایع نورپاتی ارثی شامل بیماری اس ام ای SMA و بیماری شارکو-ماری-توث Charcot-Marie-Tooth می باشد.
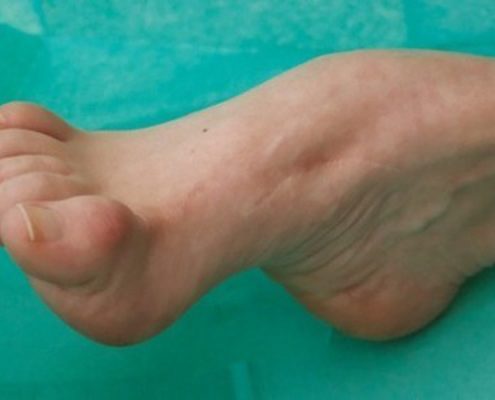
بیماری شارکو-ماری-توث چیست؟
بیماری شارکو-ماری-توث شایعترین نوع نوروپاتی ارثی است که با علایم ضعف عضلانی پیشرونده در عضلات تحتانی پاها، اختلال و مشکلات خفیف تا متوسط حسی، کاهش یا از دست دادن رفلکس های وتری اندام تحتانی و افزایش گودی کف پاها یا High Arched Feet ظاهر می شود. میزان شیوع این نورپاتی ارثی ۱ در ۲۵۰۰ نفر می باشد.
از نظر توارث ژنتیک چند نوع بیماری شارکو-ماری-توث وجود دارد؟
بیماری شارکو-ماری-توث به دو روش اتوزومال و وابسته به جنس به ارث می رسد. این بیماری شامل چندین نوع با توارث اتوزومال و یک نوع با توارث جنسی می باشد.
انواع بیماری شارکو-ماری-توث را بشناسید:
بیماری شارکو-ماری-توث تیپ ۱
شایعترین نوع بیماری شارکو-ماری-توث با شیوع ۵۰% می باشد که به صورت اتوزومال غالب به ارث می رسد. ضایعه اصلی در این بیماری آسیب به غلاف میلین رشته های عصبی محیطی است. این بیماری در دوران کودکی علایم بسیار ملایمی به صورت لاغری و ضعف در عضلات جلوی ساق پا، افزایش گودی کف پاها و کاهش رفلکی تاندون آشیل دارد. یافته نوار عصب و عضله در بیماری شارکو-ماری-توث تیپ ۱، کاهش واضح در سرعت هدایت رشته های عصبی است.
بیماری شارکو-ماری-توث تیپ ۲
بیماری شارکو-ماری-توث تیپ ۲ توارث اتوزومال غالب داشته و حدود ۳۰% انواع این بیماری را شامل می شود. علایم بالینی آن مشابه تیپ ۱ بوده ولیکن شدت علایم حسی کمتر بوده و در نوار عصب و عضله کاهش در سرعت هدایت رشته های عصبی وجود ندارد.
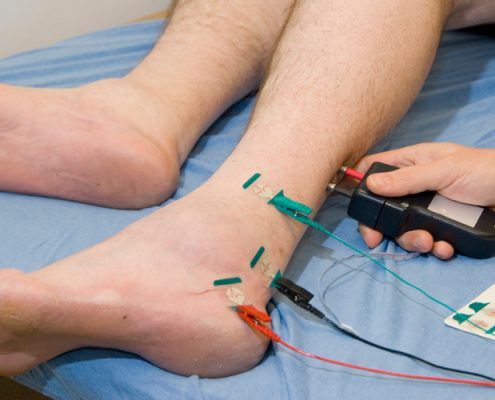
بیماری شارکو-ماری-توث تیپ ۳
سندرم Dejerine Sottas یا ۳ شدیدترین نوع بیماری شارکو-ماری-توث با بروز علایم در دوران شیرخوارگی است. آتروفی شدید عضلات، درگیری حسی و ضعف شدید علایم عمده آن می باشد.
بیماری شارکو-ماری-توث تیپ ۴
این نوع از بیماری توارث اتوزومال مغلوب داشته و همانند تیپ ۱ ضایعه غلاف میلین رشته های عصبی علت اصلی بیماری است. در بیماری شارکو-ماری-توث تیپ ۴ به نسبت تیپ ۱ علایم زودتر و با شدت بیشتری ظاهر می شود به طوری که ضعف شدید عضلات اندام تحتانی در سال دوم زندگی بروز می کند.
بیماری شارکو-ماری-توث وابسته به جنس
بیماری شارکو-ماری-توث وابسته به جنس توارث غالب داشته و در پسران مبتلا علایم شدید و در دختران مبتلا یا علامت ندارد و یا اینکه با علایم بسیار خفیف بروز می کند. شایعترین علامت این نوع بیماری شارکو-ماری-توث افتادگی پنجه پا حین راه رفتن یا Foot Drop می باشد که در پسران مبتلا قبل از ۱۰ سالگی ظاهر می شود.
روش تشخیص بیماری شارکو-ماری-توث چیست؟
بر اساس علایم بیماری شارکو-ماری-توث می توان تشخیص بیماری را انجام داد. اگرچه انجام نوار عصب و عضله و بررسی ژنتیک برای تشخیص قطعی بیماری ضروری است.